摘 要: 針對(duì)腦部血氧非侵入式無(wú)損血氧檢測(cè),設(shè)計(jì)了一款多通道的可穿戴式功能近紅外光譜成像系統(tǒng)的前端。采用超低功耗無(wú)線片上系統(tǒng)(System on a Chip,SoC)芯片作為控制中心以及無(wú)線傳送模塊,借用時(shí)分復(fù)用技術(shù)實(shí)現(xiàn)光源驅(qū)動(dòng),利用高靈敏度的光電傳感器以及高分辨率的模數(shù)轉(zhuǎn)換芯片實(shí)現(xiàn)信號(hào)采集,實(shí)現(xiàn)一款體積小、功耗低、精度高、無(wú)線數(shù)傳、可實(shí)時(shí)檢測(cè)腦部血氧濃度的系統(tǒng)前端。給出了光源驅(qū)動(dòng)與信號(hào)采集擴(kuò)展方案,使得系統(tǒng)可以自由配置成更多通道采集系統(tǒng)。
關(guān)鍵詞: 無(wú)線傳輸;可穿戴式;近紅外光譜;血氧檢測(cè);低功耗
0 引言
功能近紅外光譜技術(shù)(functional Near-Infrared Spectroscopy,fNIRS)作為一種非侵入式腦功能成像技術(shù),不僅具有安全、體積小、易于與其他設(shè)備(如腦電圖成像設(shè)備、功能核磁共振成像設(shè)備)集成[1]等優(yōu)點(diǎn),而且具有較高的時(shí)間、空間分辨率[2]。因此該技術(shù)在學(xué)術(shù)領(lǐng)域、醫(yī)療領(lǐng)域和其他社會(huì)生活領(lǐng)域的應(yīng)用研究越來越受到重視。
目前便攜式醫(yī)療設(shè)備朝著“微型化、智能化、個(gè)性化、網(wǎng)絡(luò)化”的方向發(fā)展。便攜式的fNIRS系統(tǒng)傳輸方式主要采用藍(lán)牙、ZigBee、Wi-Fi、無(wú)線射頻等無(wú)線技術(shù)。例如美國(guó)fNIR Devices公司的fNIR 1100w系統(tǒng)采用的是ZigBee技術(shù),日本日立公司2009年發(fā)布的11通道WOT系統(tǒng)采用的是802.11b無(wú)線局域網(wǎng),日本DynaSense與荷蘭Artinis公司分別基于藍(lán)牙技術(shù)開發(fā)了用于研究的雙通道與單通道設(shè)備[3]。這些國(guó)外商業(yè)系統(tǒng)主要應(yīng)用于醫(yī)院或者高校試驗(yàn)研究,且價(jià)格昂貴。國(guó)內(nèi)方面,參考文獻(xiàn)[4]、[5]分別基于無(wú)線射頻(RF)技術(shù)(工作最高速率僅20 kb/s)與GPRS技術(shù)針對(duì)肌氧檢測(cè)的便攜式設(shè)備進(jìn)行了研制,但其通道個(gè)數(shù)有限,且傳輸速率受到限制,多通道系統(tǒng)中在保證數(shù)據(jù)精度的條件下很難滿足實(shí)時(shí)數(shù)據(jù)傳輸。
本文以美國(guó)Gain-Span公司的一款高集成度、超低功耗SoC芯片GS1011為核心,設(shè)計(jì)出一款基于Wi-Fi實(shí)時(shí)無(wú)線數(shù)傳的可穿戴式fNIRS系統(tǒng)前端。
1 fNIRS技術(shù)基礎(chǔ)
1.1 生理學(xué)基礎(chǔ)
fNIRS系統(tǒng)是通過檢測(cè)血液動(dòng)力學(xué)參數(shù)間接反映神經(jīng)活動(dòng)的。ROY C S和SHERRINGTON C S于1890年針對(duì)神經(jīng)與血管間耦合關(guān)系提出了一個(gè)非常著名假說,即“大腦的血流供應(yīng)會(huì)隨其功能活動(dòng)的局部變化而進(jìn)行局部響應(yīng)”[6]。因此可以通過對(duì)血液動(dòng)力學(xué)參數(shù)檢測(cè)間接評(píng)定大腦神經(jīng)活動(dòng)。
1.2 物理學(xué)基礎(chǔ)
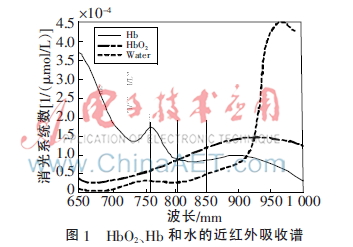
生物組織在650 nm~950 nm近紅外光譜波長(zhǎng)范圍內(nèi)呈現(xiàn)高散射、低吸收特性,因此,被稱為“光學(xué)窗口”。該波段范圍內(nèi)主要吸收光子物質(zhì)為血紅蛋白、細(xì)胞色素等,且這些物質(zhì)和占人體80%的水吸系數(shù)都比較低,允許光子從人體頭皮穿透顱骨、腦脊液等達(dá)到大腦皮層。生物組織對(duì)光吸收特性如圖1所示。
1.3 修正的Beer-Lambert定律
近紅外光在光學(xué)窗口內(nèi)能夠穿透生物組織,光子在組織中通過多次散射之后反射出皮膚。光子從光源到接收器之間大約走過一條“香蕉”形路徑,光子最大穿越深度大約為1/2倍的入射點(diǎn)與出射點(diǎn)間距離[7],其在皮膚下的傳播路徑要遠(yuǎn)大于基本的Beer-Lambert中的直線距離。
DELOY D T等人在1988年提出了平均光路長(zhǎng)和微分光路長(zhǎng)來描述光子在生物組織中的傳播路徑,并推導(dǎo)出了修正的Beer-Lambert定律[8]:
OD=ln(Io/I)=ε·DPF·l·c+G(1)
式中,ε為分子消光系數(shù)(M-1cm-1);DPF為差分路徑長(zhǎng)度因子;l為光源—探測(cè)器距離(cm);G為由皮膚、脂肪等外層組織的光學(xué)特性引起的背景散射和吸收的常數(shù)損耗因子。
臨床應(yīng)用中,通常采用光密度的相對(duì)變化量研究生物組織的光學(xué)特性,以最大程度地減小由不同生物個(gè)體的組織特性不同引起的差異。首先選取一個(gè)參考狀態(tài)作為基準(zhǔn),然后通過檢測(cè)其他狀態(tài)的變化量檢測(cè)血紅蛋白的相對(duì)變化。因此修正的Beer-Lambert定律可以改寫為:
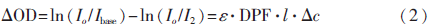
2 系統(tǒng)設(shè)計(jì)
本文研制的近紅外成像系統(tǒng)是一款反射式連續(xù)光(Continuous Wave,CW)系統(tǒng),它包括光源探頭、光源驅(qū)動(dòng)、接收器探頭、信號(hào)采集模塊、控制及無(wú)線傳送模塊、電源模塊。系統(tǒng)功能框圖如圖2所示。
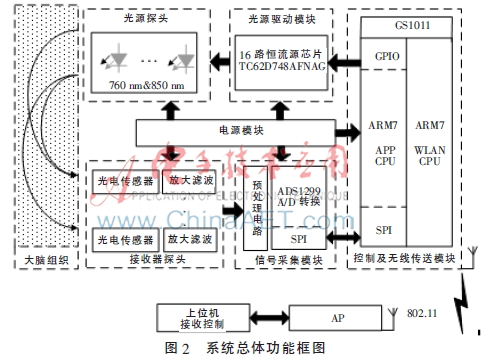
該系統(tǒng)是一個(gè)網(wǎng)絡(luò)化的嵌入式系統(tǒng),能夠?qū)崟r(shí)地檢測(cè)腦部血氧濃度變化。系統(tǒng)前端通過GS1011的Wi-Fi模塊與上位機(jī)通信,根據(jù)上位機(jī)指令協(xié)調(diào)系統(tǒng)前端工作,并通過Wi-Fi將采集到的信號(hào)傳送到指定IP地址的上位機(jī)上。另外,將復(fù)雜的數(shù)字濾波、降噪及信號(hào)分離通過高性能的上位機(jī)進(jìn)行處理,可以有效地減少系統(tǒng)前端的復(fù)雜性并提高系統(tǒng)的實(shí)時(shí)性。下面根據(jù)系統(tǒng)總體框圖中各功能模塊依次介紹系統(tǒng)的實(shí)現(xiàn)。
2.1 光源探頭設(shè)計(jì)
近紅外光譜CW成像系統(tǒng)中光源常采用分布在805 nm附近的雙波長(zhǎng)或者采用包括805 nm波長(zhǎng)的三波長(zhǎng)作為入射光。由圖1可知,在760 nm時(shí),脫氧血紅蛋白吸收系數(shù)出現(xiàn)一個(gè)吸收尖峰,因此本系統(tǒng)選取760 nm與850 nm作為入射光波長(zhǎng)。最終選用日本EPITEX公司用于醫(yī)療設(shè)備的雙波長(zhǎng)直插式LED(型號(hào):L760/850-04A),其峰值分別為760 nm和850 nm,對(duì)應(yīng)的半波長(zhǎng)分別為30 nm和35 nm。
2.2 光源驅(qū)動(dòng)設(shè)計(jì)
驅(qū)動(dòng)電流不穩(wěn)定將導(dǎo)致LED輸出功率波動(dòng),這樣就會(huì)引起輸出光強(qiáng)發(fā)生變化,從而在有用信號(hào)上疊加一個(gè)噪聲。因此,為了減小因驅(qū)動(dòng)引起的噪聲,本系統(tǒng)采用東芝公司專用LED驅(qū)動(dòng)的16路輸出恒流源芯片TC62D748。該芯片僅需要一個(gè)外接精密電阻就可固定輸出1.5~90 mA電流,具有電路簡(jiǎn)潔、控制方便等特點(diǎn),有效地減小了前端電路。
2.3 接收器探頭設(shè)計(jì)
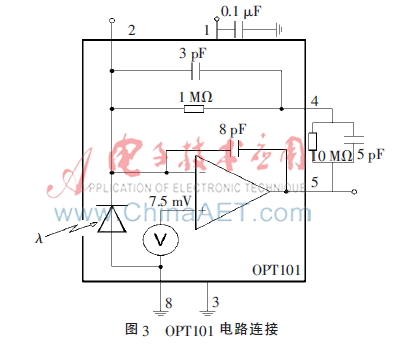
由于發(fā)射光只有十幾mV,從大腦反射出來的光在nW量級(jí),因此系統(tǒng)接收器探頭必須具有較高的靈敏度與抗干擾能力。系統(tǒng)最終采用Burr-Brown公司的光電傳感器OPT101,內(nèi)部結(jié)構(gòu)圖如圖3所示。該芯片具有以下優(yōu)點(diǎn):
(1)抗干擾能力強(qiáng)。該芯片通過將雪崩光電二極管(APD)與互阻放大器集成在一起,有效減少了雜散電容產(chǎn)生的噪聲,以及漏電流、尖峰增益等誤差。
(2)高增益。通過在引腳4、5之間外接反饋電阻電容網(wǎng)絡(luò),可以提高增益系數(shù),且由于噪聲正比于反饋電阻的平方根,因此在提高反饋電阻的同時(shí)提高了信噪比。
(3)線性度好。該傳感器具有非常好的線性響應(yīng),APD輸出100 μA時(shí)的非線性失真在0.05%以下。即使輸出1 mA時(shí),非線性度也只增加幾個(gè)百分點(diǎn)。
本系統(tǒng)通過外接10 M電阻且并聯(lián)5 pF電容組成放大反饋電路,前級(jí)電路DC增益達(dá)到11×106 V/A,-3 dB帶寬為1.3 kHz,上升時(shí)間約為270 μs。
2.4 信號(hào)采集模塊設(shè)計(jì)
本系統(tǒng)信號(hào)采集模塊采用TI公司最新推出具有高精度、低功耗、同步采樣的模數(shù)轉(zhuǎn)換芯片ADS1299。其主要優(yōu)點(diǎn)有:
(1)高分辨率,8個(gè)低噪聲三角積分模數(shù)轉(zhuǎn)換器以及可編程放大器(PGA,增益系數(shù)1~24倍可選),在轉(zhuǎn)換速率不超過8 kS/s時(shí),可以達(dá)到24 bit的分辨率,在使用內(nèi)部參考電壓VREF=4.5 V時(shí),電壓分辨率可以達(dá)到VLSB=0.536 μV。
(2)抗干擾能力強(qiáng),芯片的每路模擬輸入端有EMI濾波器,可以濾除大多高頻干擾。
(3)低功耗,芯片每個(gè)通道功耗僅5 mV,而且具有靈活的省電、待機(jī)模式,節(jié)電模式下典型功耗僅為10 μW,可以最大程度地減小功率消耗。
為了避免因頻率混疊對(duì)輸出造成的干擾,模數(shù)轉(zhuǎn)換前增加了一個(gè)低通濾波器作為預(yù)處理電路,抑制輸出信號(hào)超過奈奎斯特頻率的高頻噪聲。
2.5 控制與無(wú)線傳送模塊設(shè)計(jì)
本系統(tǒng)采用Wi-Fi作為數(shù)據(jù)傳輸技術(shù),不僅可以滿足大數(shù)據(jù)的實(shí)時(shí)傳送,而且通信距離也比較大。最終選用美國(guó)Gain-Span公司生產(chǎn)的一款高集成度、超低功耗SoC芯片GS1011。該芯片采用2.4 GHz射頻,其無(wú)線發(fā)送速率峰值高達(dá)11 Mb/s,平均速度為2 Mb/s。室內(nèi)通信范圍可以達(dá)到50~70 m,室外可以達(dá)到200 m以上。
芯片采用兩個(gè)ARM7作為處理內(nèi)核,其中一個(gè)負(fù)責(zé)無(wú)線數(shù)據(jù)傳送與接收(WLAN CPU),另一個(gè)負(fù)責(zé)應(yīng)用程序管理(APP CPU)。芯片還具有實(shí)時(shí)時(shí)鐘(Real-Time Clock,RTC)電源管理功能,能夠有效減小功耗,在待機(jī)狀態(tài)下功耗僅為15.5 μW,兩個(gè)CPU同時(shí)運(yùn)行時(shí)功耗也只有56 mW。GS1011通過SPI口控制ADS1299采集以及接收模數(shù)轉(zhuǎn)換后的信號(hào),通過GPIO口控制恒流源芯片按照時(shí)序邏輯輸出電流。
3 系統(tǒng)擴(kuò)展
本系統(tǒng)基本配置為8個(gè)光源,8個(gè)探測(cè)器組成的8通道系統(tǒng)可以根據(jù)實(shí)際需求自由擴(kuò)展。下面分別給出了16路通道的級(jí)聯(lián)模式示意圖,光源驅(qū)動(dòng)擴(kuò)展如圖4所示,信號(hào)采集擴(kuò)展如圖5所示。

4 結(jié)論
本文以近紅外光譜技術(shù)血氧檢測(cè)機(jī)理為基礎(chǔ),設(shè)計(jì)了一款可以自由配置通道個(gè)數(shù)的血氧檢測(cè)系統(tǒng)前端。為了實(shí)現(xiàn)可穿戴式設(shè)備的要求,本文針對(duì)系統(tǒng)的便攜性、低功耗、無(wú)線數(shù)傳進(jìn)行了重點(diǎn)研究。通過使用低功耗、高集成度芯片,使得整個(gè)系統(tǒng)體積小、重量輕、精度高、可自由移動(dòng),并且系統(tǒng)可以實(shí)時(shí)傳送數(shù)據(jù)。突破了臺(tái)式檢測(cè)設(shè)備的應(yīng)用領(lǐng)域,以及常規(guī)無(wú)線技術(shù)對(duì)數(shù)據(jù)傳送速率的限制,適用于兒童、老人、認(rèn)知心理學(xué)等領(lǐng)域的腦部實(shí)時(shí)血氧檢測(cè)。
參考文獻(xiàn)
[1] PIPER S K, KRUEGER A, KOCH S P, et al. A wearable multi-channel fNIRS system for brain imaging in freely moving subjects[J]. NeuroImage, 2014(85):64-71.
[2] STRANGMAN G, BOAS D A, SUTTON J P. Non-invasive neuroimaging using near-infrared light[J]. Biological psychiatry, 2002,52(7):679-693.
[3] FERRARI M, QUARESIMA V. A brief review on the history of human functional near-infrared spectroscopy (fNIRS) development and fields of application[J]. Neuroimage, 2012,63(2):921-935.
[4] 劉方,駱清銘,李鵬程,等.基于RF無(wú)線數(shù)據(jù)傳輸技術(shù)的近紅外血氧監(jiān)測(cè)儀的研制[J].中國(guó)醫(yī)療器械雜志,2003(3):162-166.
[5] 陳剛.基于GPRS無(wú)線肌氧檢測(cè)系統(tǒng)的研制及應(yīng)用[D].武漢:華中科技大學(xué),2005.
[6] ROY C S, SHERRINGTON C S. On the regulation of the blood-supply of the brain[J]. The Journal of Physiology, 1890,11(1-2):85.
[7] 張巖.基于近紅外光譜技術(shù)的腦功能活動(dòng)信號(hào)提取方法研究[D].哈爾濱:哈爾濱工業(yè)大學(xué),2011.
[8] DELPY D T, COPE M, VAN DER ZEE P, et al. Estimation of optical pathlength through tissue from direct time of flight measurement[J]. Physics in Medicine and Biology, 1988,33(12):1433.

