研究人員已經(jīng)創(chuàng)造出了新的鉆形納米材料,它們可以滲透細胞膜并在細胞內(nèi)傳遞藥物,從而提供了一種提高治療功效的通用手段。他們的工作發(fā)表在《受控釋放雜志》上。
開發(fā)有效的治療藥物是一個艱巨的過程,甚至在臨床試驗開始之前就需要大量的時間和金錢。通常,從理論上講應該治療疾病的藥物無法進行臨床試驗,因為這些藥物無法穿透生物屏障(例如細胞膜)并無法達到所需的分子靶標。
俄勒岡州立大學的科學家開發(fā)了一種新的納米材料,該材料可促進藥物通過細胞膜(稱為CSPNs)或可穿透細胞的自組裝肽納米材料的傳遞。這些納米結(jié)構(gòu)由自組裝成類似于鉆頭形狀的氨基酸組成,這些納米結(jié)構(gòu)可以包裹藥物,在滲透膜后將其輸送到細胞中。CSPNs還具有高度的通用性,可以進行修改以適應特定的藥理需要。
研究負責人Gaurav Sahay說:“ CSPNs是一種新的模塊化藥物遞送平臺,可以通過氨基酸的序列特異性微調(diào)將其編程為精美的結(jié)構(gòu)。”“氨基酸的微調(diào)賦予了其多種功能,例如柔韌性,自組裝性,更高的載藥量,可生物降解性和生物相容性,可實現(xiàn)CSPN的有效細胞內(nèi)遞送。”
研究人員測試了5種不同的CSPN的結(jié)構(gòu)和功能,他們通過將肽與(RADA)2接頭綴合并改變其中包含的苯丙氨酸殘基的數(shù)量來構(gòu)建它們。
“我們之所以選擇(RADA)2,是因為它含有可排斥水并與水混合的交替氨基酸;主要作者Ashwani Narayana評論道。“我們證明了這些CSPN中二級結(jié)構(gòu)的轉(zhuǎn)變,這反過來在自組裝和藥物輸送潛力中起著至關重要的作用。這些納米鉆的體內(nèi)功效將使邊界擴展到細胞內(nèi)傳遞之外。”納里亞納補充說。
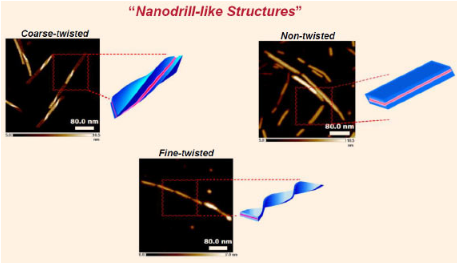
有趣的是,他們發(fā)現(xiàn)CSPNs的形狀從粗捻到細捻的納米鉆形態(tài)有所變化,因為它們添加了更多的苯丙氨酸殘基。
粗麻花鉆有效地輸送了雷帕霉素,雷帕霉素是一種眾所周知的誘導自噬的藥物,可回收細胞成分。Narayana說:“這些納米鉆具有很高的封裝疏水性客體分子的能力。” “特別是粗扭曲的納米鉆顯示出更高的內(nèi)在化,并且能夠在小鼠模型中將雷帕霉素定位在肝臟中。”
這些模塊化的CSPN可能是一個跨分子屏障傳遞分子的新平臺。微小的變化可以將自組裝引導為無數(shù)定義的納米結(jié)構(gòu),使其成為一系列不同分子的理想宿主。

