天上若無(wú)難走路,世間哪個(gè)不成仙?上篇我們聊了聊作為電動(dòng)汽車(chē)關(guān)鍵技術(shù)也是難點(diǎn)的動(dòng)力電池的主要性能參數(shù)。最近討論比較多的就是 BYD 的刀片電池,以及這兩天剛看到的廣汽的"石墨烯電池",8 分鐘充電 85%也是很厲害了,但是具體是石墨烯還是石墨烯基電池就說(shuō)不大準(zhǔn)了。今天我們不聊刀片也不談石墨烯,我們來(lái)看看動(dòng)力電池的主要類(lèi)型有哪些~
電動(dòng)汽車(chē)用動(dòng)力電池主要有鉛酸蓄電池、金屬氫化物鎳蓄電池、鋰離子蓄電池、鋅空氣電池、超級(jí)電容器等。
鉛酸蓄電池
鉛酸蓄電池指的是二氧化鉛作為正極,海綿狀鉛作為負(fù)極,以硫酸溶液作為電解液的蓄電池,其主要用在低速電動(dòng)車(chē)上。

正負(fù)極板:正極二氧化鉛,負(fù)極海綿狀純鉛;
隔板:隔離正、負(fù)極板以防短路,同時(shí)作為電解液的載體,吸收了大量的電解液,促進(jìn)離子更好地?cái)U(kuò)散;
電解液:純硫酸和蒸餾水配制的一定比例的硫酸;
溢氣閥:位于蓄電池頂部,起安全、密封、防爆作用;
化學(xué)能和電能的轉(zhuǎn)換我們稱(chēng)為充放電,鉛酸蓄電池屬于酸性電池,其化學(xué)反應(yīng)式為:PbO+H2SO4→PbSO4+H2O

充電時(shí),把鉛板分別和直流電源的正負(fù)極相連,進(jìn)行電解(氧化還原反應(yīng)),陰極為還原反應(yīng),陽(yáng)極為氧化反應(yīng):
陰極:PbSO4+2eˉ→Pb+SO42ˉ
陽(yáng)極:PbSO4+2H2O→PbO2+4H++SO42ˉ+2eˉ
充電時(shí)的總反應(yīng):2PbSO4+2H2O→Pb+PbO2+2H2SO4
隨著電流通過(guò),PbSO4 在陰極上變成蓬松的金屬鉛,在陽(yáng)極變成黑褐色的二氧化鉛,溶液中有 H2SO4 產(chǎn)生。
放電時(shí),陽(yáng)極還原反應(yīng):
陽(yáng)極:PbO2+4H++2eˉ→Pb2++2H2O
由于硫酸的存在,Pb2+也立即生成 PbSO4。
放電時(shí)的總反應(yīng):Pb+PbO2+2H2SO4→2PbSO4+2H2O
蓄電池充電時(shí),隨著電池端電壓的升高,水開(kāi)始被電解,當(dāng)單體電池電壓達(dá)到 2.4V 左右時(shí),水的電解不可忽視。水電解時(shí)陽(yáng)極和陰極反應(yīng)分別為:
陽(yáng)極:H2O→1/2O2+2H++2eˉ
陰極:2H++2eˉ→H2
陽(yáng)極給出電子,陰極得到電子,形成回路電流。端電壓越高,電解水也就越激烈,此時(shí)充入的大部分電荷參加水電解,形成的活性物質(zhì)很少了。
電動(dòng)汽車(chē)對(duì)鉛酸蓄電池的要求:
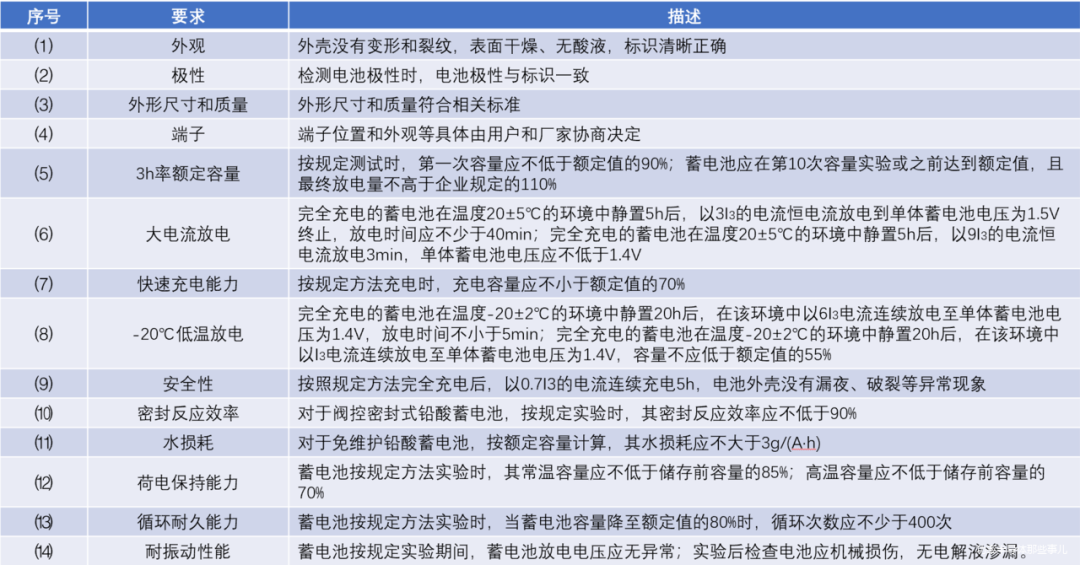
金屬氫化物鎳蓄電池
金屬氫化物鎳蓄電池,也叫作氫鎳蓄電池,指的是正極為鎳氧化物,負(fù)極為可吸收釋放氫的儲(chǔ)氫合金,以氫氧化鉀為電解質(zhì)的蓄電池。氫鎳蓄電池大多應(yīng)用在混合動(dòng)力電動(dòng)汽車(chē)上,可分為方形和圓柱形兩種。
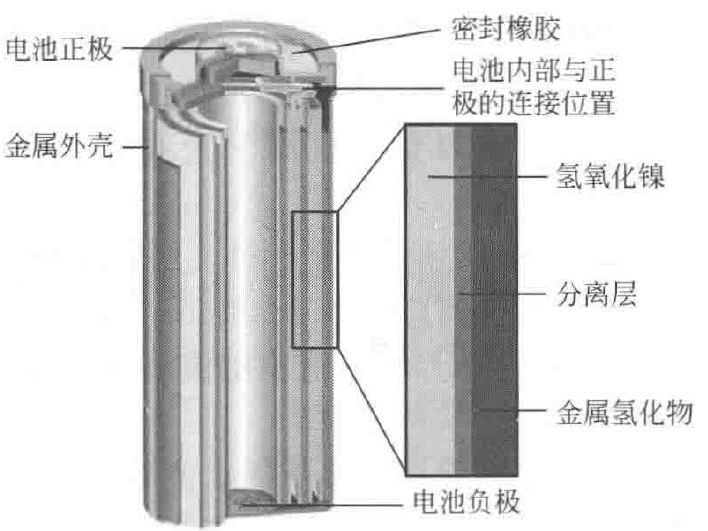
如上圖,圓柱形氫鎳蓄電池,主要包括正極(氫氧化鎳)、負(fù)極(儲(chǔ)氫合金)、分離層(隔膜紙)、外殼、電解液(氫氧化鉀)等,在金屬鉑的催化作用下,完成充電和放電的可逆反應(yīng)。圓柱形電池中,正負(fù)極由隔膜紙分開(kāi)卷繞在一起,然后密封在金屬外殼中。方形電池中,正負(fù)極由隔膜紙分開(kāi)后疊成層狀密封在外殼兒中。
金屬氫化物鎳蓄電池的性能特點(diǎn)取決于本身體系的電極反應(yīng),充電時(shí),
正極:Ni(OH)2-eˉ+OHˉ→NiOOH+H2O
負(fù)極:2MH+2eˉ→2Mˉ→2Mˉ+H2
放電時(shí),
正極:NiOOH+H2O+eˉ→Ni(OH)2+OHˉ
負(fù)極:2Mˉ+H2→Ni(OH)2+OHˉ
對(duì)氫鎳蓄電池的要求分為單體蓄電池的要求和蓄電池模塊的要求。
對(duì)氫鎳蓄電池的單體電池的要求:

對(duì)氫鎳蓄電池模塊的要求:

還剩下另外三種電動(dòng)汽車(chē)主要的動(dòng)力電池類(lèi)型我們明天再聊,今天的內(nèi)容希望你們能夠喜歡。

